Workflow en radioterapia adyuvante para cáncer de mama
En España se diagnostican unos 35.000 nuevos casos de cáncer de mama al año y la supervivencia media a 5 años es superior al 80%, siendo de los mejores resultados de toda Europa. Ello es debido a la generalización de los programas de cribado poblacional y a las mejoras en el tratamiento, tanto locorregional como sistémico. El manejo de cada paciente depende del estadio de la enfermedad, y se estima que el 80% de las pacientes con cáncer de mama recibirán radioterapia (RT) en algún momento de la evolución de su enfermedad, tanto con intención radical como paliativa para control de síntomas.
La gran mayoría de pacientes tratadas con RT lo hacen como complemento tras la cirugía conservadora que, en carcinoma infiltrante de mama, hace referencia a la exéresis de la lesión tumoral con márgenes libres mas biopsia selectiva del ganglio centinela (BSGC) o linfadenectomía axilar, pero manteniendo la integridad de la mama.
La RT complementaria tras este tipo de cirugía va a estar indicada en casi todos los casos, y el objetivo es erradicar la posible enfermedad microscópica, habiendo demostrado que:
-Disminuye el riesgo de recurrencia locorregional
-Mejora la supervivencia cáncer específica
Normalmente se administra tras la cirugía, pero si se va a recibir quimioterapia adyuvante, habitualmente se administra tras finalizar este tratamiento sistémico. Aunque el intervalo óptimo desde la cirugía conservadora a la irradiación no está 100% definido, la mayoría de guías y estudios indican que la irradiación debe comenzar dentro de las 12 semanas después de la cirugía, aunque este tiempo normalmente se demorará en los casos en los que se realice tratamiento sistémico tras la cirugía.
Una vez aprobada la indicación de RT, habrá que decidir qué técnica utilizar en cada caso, que se realizará de forma individualizada y según disponibilidad en cada centro, Radioterapia Intraoperatoria o RIO, braquiterapia intersticial, o bien Radioterapia Externa -RTE-. Esta última es la técnica más habitual y en la que nos vamos a centrar.
Así que, ¿cuáles son los pasos a seguir cuando se indica tratamiento con RTE?
1.Consulta inicial: se trata de una consulta informativa en la que tu oncólogo radioterápico te explicará todo el proceso y resolverá las dudas que puedan surgir.
2.TAC de Simulación: realización de un TAC que comprende el área a tratar y que normalmente no requiere estar en ayunas (se realiza sin contraste intravenoso). Este TAC no es diagnóstico como tal con lo que no llevará ningún informe asociado, y servirá al oncólogo radioterápico como una “copia anatómica” para poder planificar el tratamiento. Aunque ya hay sistemas donde se puede obviar, lo más extendido es la realización de 3 puntitos de tatuaje que sirven como localizadores y que quedan localizados bajo el esternón y en ambos lados del tórax; se trata de tatuajes en forma de pequeños lunares que no se borrarán.
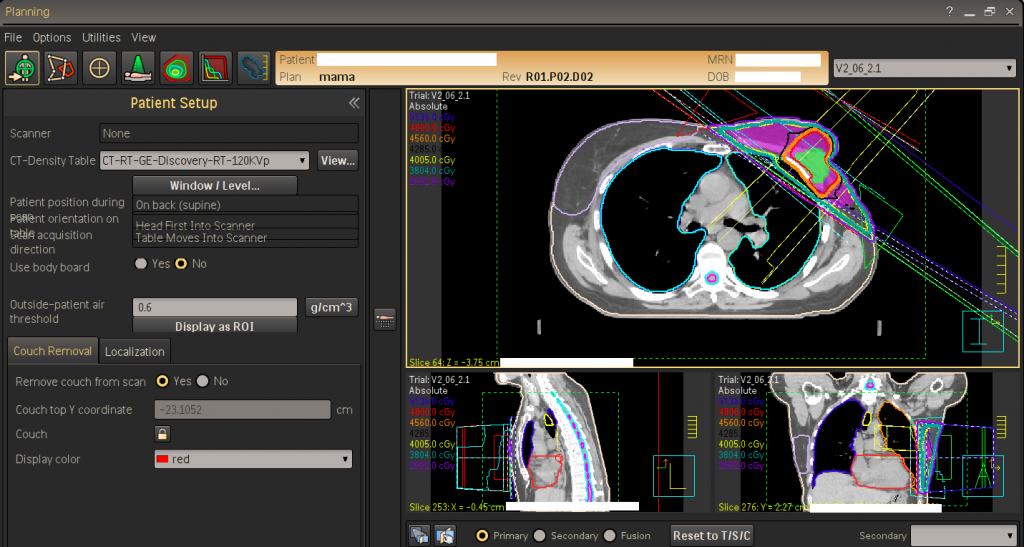
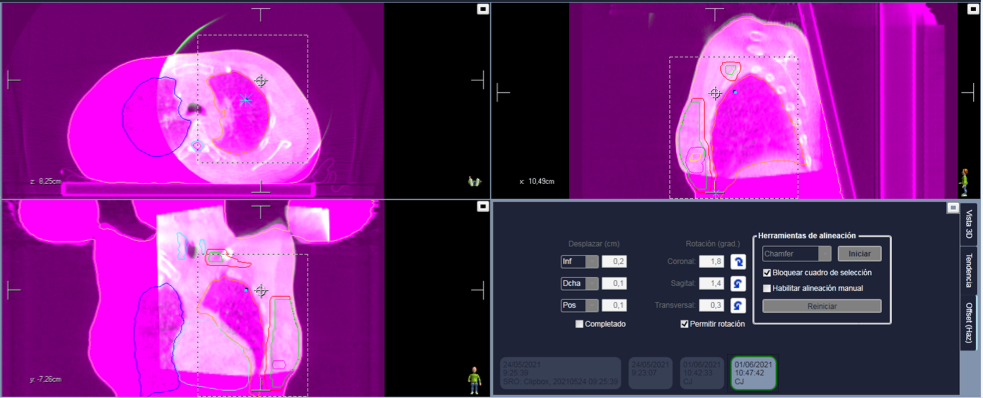
3.Planificación: esta parte de trabajo conjunto entre los Servicios de Oncología Radioterápica y Radiofísica es la menos conocida y, sin duda, una de las más importantes. La tarea del oncólogo radioterápico, además de la elección de la dosis a administrar y del esquema de tratamiento a seguir, consistirá en evaluar ese TAC inicial y delimitar qué volúmenes queremos tratar así como todos aquellos órganos y estructuras cercanas cuya integridad queremos preservar. Posteriormente, será el radiofísico quien se encargue de elaborar una planificación para hacer que la radiación alcance todos los volúmenes indicados por el médico, protegiendo lo que conocemos como órganos de riesgo en base a unos límites de tolerancia de cada tejido ya prefijados. Una vez finalizada la planificación, será necesario aprobar (o rechazar y repetir si así se considera) la misma por parte del médico comprobando que se cumplen los estándares de calidad.
4.Puesta de tratamiento: tras ese margen de tiempo de planificación, el tratamiento está listo para empezar y se realiza la primera sesión de tratamiento, que suele llevar algo más de tiempo que las posteriores puesto que se debe comprobar que todo está en orden.
5.Sesiones: cada sesión dura aproximadamente 10 minutos y es indolora, y durante la misma se suelen realizar sobre la marcha imágenes de comprobación (lo que conocemos como IGRT o radioterapia guiada por imagen) de forma que nos aseguramos casi diariamente de que el tratamiento es correcto; si en algún momento se detectan variaciones (por incremento o descenso de peso que modifique la anatomía, cambios en el volumen de área tumoral, etc.) podremos plantear la replanificación del tratamiento en base a esas nuevas circunstancias. A destacar que la radiación no se ve, no quema y no te hará ser radiactiva, con
lo que puedes estar en contacto con sin ningún problema. Las sesiones suelen ser diarias de L a V, y el número de sesiones definitivo será individualizado en cada caso.
6.Seguimiento: durante el tratamiento habrá consultas programadas para evaluar posibles efectos secundarios y atención directa fuera de consulta para cualquier evento o duda que pueda surgir en relación al tratamiento. Una vez finalizado el tratamiento, se iniciará el periodo de revisiones periódicas en consulta.
Prohibido quedarse con dudas, ¡os toca preguntar!
Rosario Ching López
Oncóloga radioterápica, Hospital Universitario Virgen de las Nieves, Granada.
Master en Oncología Ginecológica.
Experto en Medicina Estética Oncológica
Fuentes:
SEOM. Las cifras del cáncer en España–2021.
Early Breast Cancer Trialists’ Collaborative Group (EBCTCG), Darby S, McGale P. Effect of radiotherapy after breast-conserving surgery on 10-yea rrecurrence and 15-year breast cancer death: metaanalysis of individual patient data for 10,801 women in 17 randomised trials. Lancet. 2011 Nov; 378 (9804): 1707-16.
Galimberti V, Cole BF, Zurrida S, Viale G, Luini A, Veronesi P, et al. Axillary dissection versus no axillary dissection in patients with sentinelnodemicrometastases (IBCSG 23-01): a phase 3 randomised controlled trial. Lancet Oncol. 2013; 14 (4): 297–305.
Galimberti V, Cole BF, Viale G, Veronesi P, Vicini E, Intra M, Mazzarol G et al. Axillary dissection versus no axillary dissection in patients with breast cáncer and sentinel node micrometastases (IBCSG 23-01): 10-year follow-up of a randomised, controlled phase 3 trial. Lancet Oncol. 2018 Oct; 19 (10): 1385- 1393.
Giuliano AE, Hunt KK, Ballman KV, Beitsch PD, Whitworth PW, Blumencranz PW, et al. Axillary dissection vs no axillary dissection in women with invasive breast cancer and sentinel node metastasis: a randomized clinical trial. JAMA. 2011; 305 (6): 569–75.
Giuliano AE, Ballman KV, McCall L, Beitsch PD, Brennan MB, Kelemen PR et al. Effect of Axillary Dissection vs No Axillary Dissection on 10-YearOverall Survival Among Women With Invasive Breast Cancer and Sentinel Node Metastasis: The ACOSOG Z0011 (Alliance) Randomized Clinical Trial. JAMA. 2017 Sep 12; 318 (10): 918-926.
Donker M, van Tienhoven G, Straver ME, Meijne P, van de Velde CJ, Mansel RE, Cataliotti L et al. Radiotherapy or surgery of the axilla after a positive sentinel node in breast cancer (EORTC 10981-22023 AMAROS): a randomised, multicentre, open-label,phase 3 non-inferiority trial. Lancet Oncol. 2014 Nov; 15 (12): 1303-10.



