El National Cancer Institute define la terapia biológica como ‘aquella terapia que implica el uso de organismos vivos o de sustancias procedentes de éstos (o sus versiones producidas en el laboratorio) para tratar enfermedades’. (1, 2) Según la FDA (Food and Drug Administration), el concepto de fármaco biológico o biofármaco abarca todos los preparados formados por péptidos o proteínas, ácidos nucleicos, azúcares e incluso por células y tejidos usados para este fin. En este artículo se hará hincapié en las ventajas de este tipo de terapia, comparada con la terapia tradicional para el cáncer, así como en los anticuerpos monoclonales, un tipo de fármacos biológicos que han supuesto una auténtica revolución en el tratamiento de ciertos tipos de cáncer.

´
Los medicamentos biológicos poseen importantes ventajas (Tabla 1) frente a los compuestos utilizados tradicionalmente, también conocidos como moléculas pequeñas o small molecules. La ventaja principal es la mayor especificidad, que es posible gracias a la elevada complejidad y al parecido molecular de los biológicos con las moléculas endógenas, lo que se traduce en una disminución de la frecuencia de efectos adversos en el paciente, teniendo por tanto un mejor perfil de seguridad. Para entenderlo mejor, podemos pensar que cuanto más pequeña y simple es una molécula (como las moléculas empleadas en quimioterapia) más facilidad va a tener para atravesar membranas y barreras celulares, así como para unirse a cualquier sitio con el que comparta propiedades fisicoquímicas parecidas.
Por tanto, se consigue dirigir el fármaco solo hacia aquellas células enfermas, deteniendo su progresión y modificando el curso de la enfermedad a pronósticos más favorables. Comparada con la quimioterapia tradicional para el cáncer, la terapia biológica supone una mejora en la calidad de vida del paciente oncológico(3) , puesto que logra solucionar el inconveniente principal de los fármacos citostáticos. En contraposición, la terapia biológica conlleva un riesgo de reacciones inmunológicas graves relacionadas precisamente con su mecanismo de acción, pero que, como se ha mencionado anteriormente, se dan con mucha menos frecuencia que las reacciones adversas con quimioterapia tradicional.
Como inconvenientes, también debido a su naturaleza, los fármacos biológicos son más sensibles a cambios de temperatura, luz o la acción de algunas enzimas fisiológicas, y se verán inactivados de ser sometidos a tales ambientes. Debido a esto, tanto los métodos de producción como la tecnología de administración se ven dificultados. Por su parte, la producción industrial ha de verse sometida a controles específicos que aseguren la óptima obtención de estos fármacos, así como es necesario que existan métodos de caracterización que definan las propiedades fisicoquímicas, lo que conlleva a un encarecimiento general en la producción si se compara con los métodos tradicionales de síntesis química.(4) En cuanto a la tecnología de administración, actualmente la gran mayoría de moléculas biológicas terapéuticas han de ser administradas por vías parenterales que conllevan dolor e incomodidad en el paciente, pero que son las únicas que aseguran la biodisponibilidad necesaria (cantidad de fármaco que llega a la circulación general en comparación con la cantidad de fármaco administrada).
Es innegable que los fármacos biológicos están desempeñando una función esencial en el tratamiento del cáncer, siendo ésta su aplicación terapéutica principal. De todos los tipos de biofármacos, los anticuerpos monoclonales fueron los más comercializados en 2018; aunque terapias con ácidos nucleicos (como terapia génica y otras terapias que incluyen RNA de interferencia) y con líneas celulares experimentaron un crecimiento significativo el pasado año (5). Por ello, he querido incluir una visión algo más profunda en los anticuerpos monoclonales a continuación.
Anticuerpos monoclonales
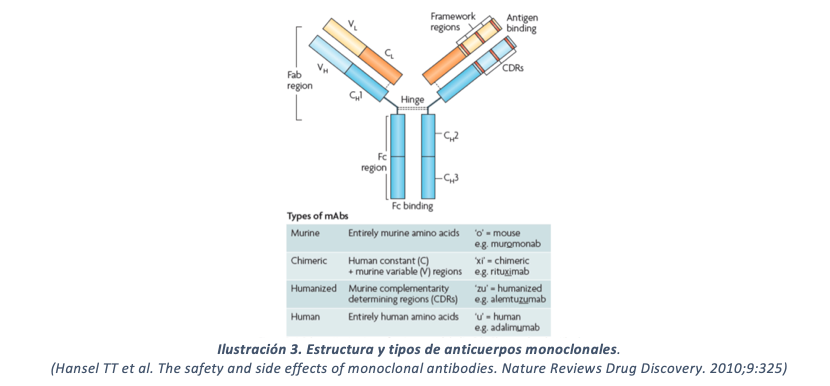
Los anticuerpos monoclonales son proteínas globulares grandes que presentan dos subunidades, Fc y Fab. Dentro de estas dos subunidades, los anticuerpos pueden presentar diferentes subregiones. Dependiendo del origen (humano o de ratón) de estas subregiones los anticuerpos monoclonales se dividen en murinos, quiméricos, humanizados y humanos (Ilustración 3) (6-8).
¿Cómo funcionan?
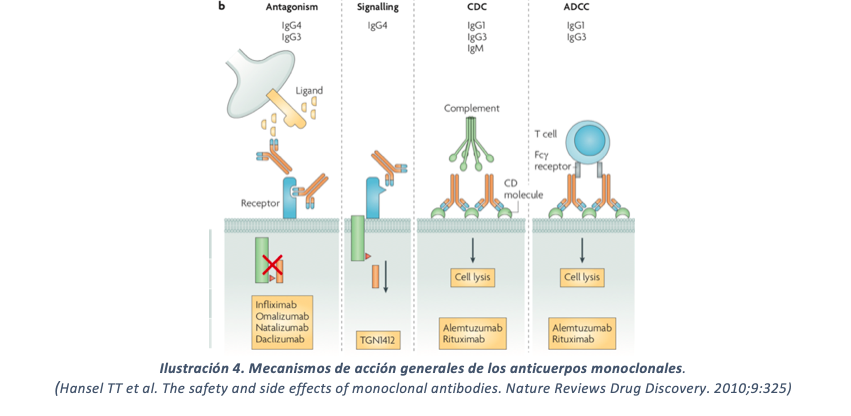
El mecanismo general de los anticuerpos consiste en la unión de la subunidad Fab (concretamente por las regiones CDR) a receptores celulares que están implicados en vías de señalización relacionadas con la patología. Esta unión impide, en primer caso, que el ligando endógeno interaccione y active la cascada de señalización (parando así el crecimiento y diferenciación de estas células enfermas), mientras que, a la vez, la interacción de la región Fc con otros componentes del sistema inmunitario (células inmunitarias o moléculas del complemento, entre otras) activa señales que desencadenan un ataque del sistema inmunitario sólo a estas células cancerosas. En contrapartida, estos fármacos sólo podrán ser utilizados en pacientes que expresen esos receptores en sus células oncológicas, algo que no ocurre en todos los tipos de tumores; lo que explica que hoy en día la quimioterapia tradicional es todavía muy necesaria.
Así, el mecanismo de acción de estas macromoléculas no se basa en una sola interacción, sino en un conjunto de estas que potencian la acción del sistema inmunitario contra las células cancerosas (Ilustración 4). Asimismo, los anticuerpos pueden ser administrados desnudos o unidos a fármacos citotóxicos, en cuyo caso la función del anticuerpo es además transportadora.(6, 7)
En cáncer, el objetivo es inducir la destrucción de las células del tumor, ya sea de manera directa o indirecta; dirigiendo el fármaco hacia dianas en las propias células o en los vasos sanguíneos que nutren el tumor. Actualmente, dos de las dianas terapéuticas más conocidas y utilizadas son el receptor HER2/neu y el MUC1, utilizadas en cáncer de mama – trastuzumab – y cáncer colorrectal, entre otros, – bevacizumab – respectivamente (8). Cetuximab, por su parte, inhibe el factor de crecimiento epidérmico (EGFR) y ha demostrado su eficacia para cáncer colorrectal positivo en este receptor (7).
Como conclusión, es importante resaltar que ambas terapias se utilizan en la actualidad, incluso en algunos casos se complementan; y aunque el futuro se dirige hacia los fármacos biológicos, en los casos en los que aún no se puede utilizar, el uso de citostáticos es necesario.

Laura Taina González (@farmaciaconlaura)
Farmacéutica.
BIBLIOGRAFÍA
1. National Cancer Institute E. Inmunoterapia Estados Unidos de América: National Cancer Institute; 2018 [Available from: https://www.cancer.gov/espanol/cancer/tratamiento/tipos/inmunoterapia.
2. National Cancer Institute E. Terapia dirigida para tratar cáncer. Estados Unidos de América: National Cancer Institute; 2018 [Available from: National Cancer Institute.
3. Vllasaliu D. Peptide and protein delivery by injection. King’s College London, London. 2018.
4. Morrow T, Felcone LH. Defining the difference: What Makes Biologics Unique. Biotechnology healthcare. 2004;1(4):24-9.
5. Walsh G. Biopharmaceutical benchmarks 2018. Nature Biotechnology. 2018;36:1136.
6. Hansel TT, Kropshofer H, Singer T, Mitchell JA, George AJT. The safety and side effects of monoclonal antibodies. Nature Reviews Drug Discovery. 2010;9:325.
7. Thurston D. Antibody-Based Approaches to Tumour Targeting. King’s College London, London, UK2018.
8. Brekke OH, Sandlie I. Therapeutic antibodies for human disease at the dawn of the twenty-first century. Nature Reviews Drug Discovery. 2003;2:240.